¡Tu solución está lista!
Nuestra ayuda de expertos desglosó tu problema en una solución confiable y fácil de entender.
Mira la respuestaMira la respuesta done loadingPregunta: SeContestaSe oxida metano (CH4) con aire para producir 120molh de formaldehído (HCHO) en un reactorcontinuo,CH4(g)+O2(g)longrightarrowHCHO(g)+H2O(v)La reacción principal (ec. anterior) compite con la combustión de metano para formar CO2(g)yH2O(v)Se tiene la siguiente información:Se producen 3 mol de HCHO por cada 4 mol de CH4 consumidas,La conversión
SeContestaSe oxida metano con aire para producir de formaldehdo en un reactorcontinuo,La reaccin principal ec anterior compite con la combustin de metano para formarSe tiene la siguiente informacin:Se producen mol de HCHO por cada mol de consumidas,La conversin de metano es delEl oxgeno se alimenta con un de exceso respecto a la reaccin principal como si sloocurriera la rxn principalEl aire se compone del de oxgeno y nitrgenoEl metano se alimenta a y el aire aLa corriente gaseosa que deja el reactor se encuentra aDetermina,a el flujo molar del alimentadob el flujo molar de salida delc el flujo molar de salida deld el calor que debe suministrarse o retirarse del reactor kWNotas:Usa el mtodo de calor de reaccinoxida metano con aire para producir de formaldehdo en un reactorcontinuo,La reaccin principal ec anterior compite con la combustin de metano para formar ySe tiene la siguiente informacin:Se producen mol de HCHO por cada mol de consumidas,La conversin de metano es delEl oxgeno se alimenta con un de exceso respecto a la reaccin principal como si sloocurriera la rxn principalEl aire se compone del de oxgeno y nitrgenoEl metano se alimenta a y el aire aLa corriente gaseosa que deja el reactor se encuentra aDetermina,a el flujo molar del alimentadob el flujo molar de salida delc el flujo molar de salida deld el calor que debe suministrarse o retirarse del reactor kWNotas:Usa el mtodo de calor de reaccin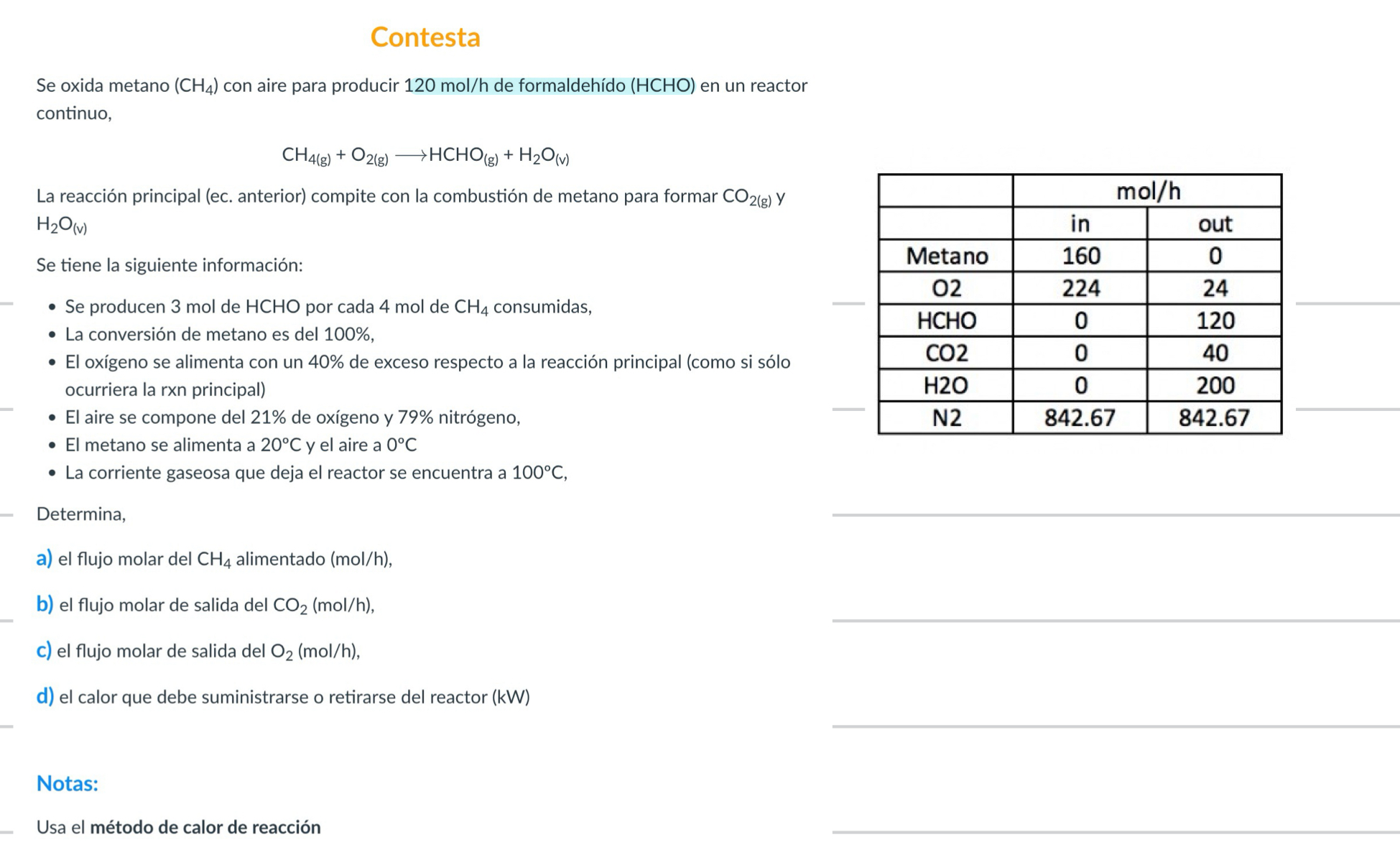
- Hay 2 pasos para resolver este problema.SoluciónPaso 1Mira la respuesta completa
Este problema se basa en la oxidación del metano
 DesbloqueaRespuestaDesbloquea
DesbloqueaRespuestaDesbloquea

Estudia mejor, ¡ahora en español!
Entiende todos los problemas con explicaciones al instante y pasos fáciles de aprender de la mano de expertos reales.