Pregunta: \# de muestra: Nombredelantiścido. \begin{tabular}{|l|l|l|l|} \hline & \multicolumn{2}{|c|}{ Prueba } \\ \hline & I & 2 & \\ \hline Peso pastilla de antiácido & & & \\ \hline Volumen añadido de ácido & & & \\ \hline Lectura inicial de la bureta & & & \\ \hline Lectura final de la bureta & & & \\ \hline Volumen de NaOH usado & & & \\ \hline ¿Cuaˊntos moles
Prueba 1:Peso de pastilla de antiacido= 1.2637 gVolumen añadído de acido= 0.075 LLectura inicial de la bureta= 0.001mlLectura final de la bureta= 1.01mlVolumen de NaOH usado= 1.01mlMoles de HCL que se añadieron al inicio del experimento en la muestra= 0.315Moles de NaOH que reaccionaron con el sobrante= 0.004Moles de HCL que reaccionaron con el antiácido= 0.311Prueba 2:Peso de pastilla de antiacido= 1.1687Volumen añadído de acido= 0.075 LLectura inicial de la bureta= 1.01mlLectura final de la bureta= 24.07 mlVolumen de NaOH usado= 24.07mlMoles de HCL que se añadieron al inicio del experimento en la muestra= 0.315Moles de NaOH que reaccionaron con el sobrante= 0.096Moles de HCL que reaccionaron con el antiácido= 0.219Prueba 3:Peso de pastilla de antiacido= 0.7286 gVolumen añadído de acido= 0.075 LLectura inicial de la bureta= 24.07 mlLectura final de la bureta= 26.02 mlVolumen de NaOH usado= 20.02 mlMoles de HCL que se añadieron al inicio del experimento en la muestra= 0.315Moles de NaOH que reaccionaron con el sobrante= 0.10Moles de HCL que reaccionaron con el antiácido= 0.215- Esta pregunta aún no se resolvió!¿No es lo que buscas?Envía tu pregunta a un experto en la materia.Texto de la transcripción de la imagen:\# de muestra: Nombredelantiścido. \begin{tabular}{|l|l|l|l|} \hline & \multicolumn{2}{|c|}{ Prueba } \\ \hline & I & 2 & \\ \hline Peso pastilla de antiácido & & & \\ \hline Volumen añadido de ácido & & & \\ \hline Lectura inicial de la bureta & & & \\ \hline Lectura final de la bureta & & & \\ \hline Volumen de NaOH usado & & & \\ \hline ¿Cuaˊntos moles de HCl se anadieron al inicio del experimento en la muestra? & & & \\ \hline ¿Cuaˊntos moles de NaOH reaceionaron con el sobrante de HCl? & & & \\ \hline ¿Cuảntos moles de HCl reaccionaron con el antiaˊcido? & & & \\ \hline \end{tabular} C.N.= ar de antiacido mmoles de H+que reaccionaxon Deferoune la estadistica de la capacidad neumalizante del aniacifo. En el informe incluya: 1. ¿Qué es una titulncióno valoraciòn pđaretroceso? ¿Por qué se utilizan? 2. ¿Qué volumen del HCl que usted aĥadió reaccionafon con el antiácido? Utilizando la Capacidad Neutralizante proenedio que usted obtuvo, responda las preguntas 3 y 4 3. «Caăntos ml de HCl serain nececanos para neutralizar I g de antiàcidoy 4. Si el fabricante de la pastilla que ustedes atilizaron en el experimento recomienda utilizar 2 pastillas cada vez que se tienen los sintomas asumicndo que cada pastilla pesa 1.4gr.cn total. a. LCuintos milimolex de HCT se neutralizarain? b. LCuänos ml del HCl utilizado en el lab se ncutratizariar?. 5. Por que se debe hervir la soluciòn anter de la tialacion'? 6. Como serian los motes de HiCl que resceionan (maborss, rucnores o igualev) a Ia solición no se hicrve? 7. Un antiacido tiene una cipacidad betual izancede 3 milanolos. H. gr. Companaido. 8. Si el aritiacido evia expicito? a. Alectara la precisiàn de aus rexaltados? tabeicent
Texto de la transcripción de la imagen:
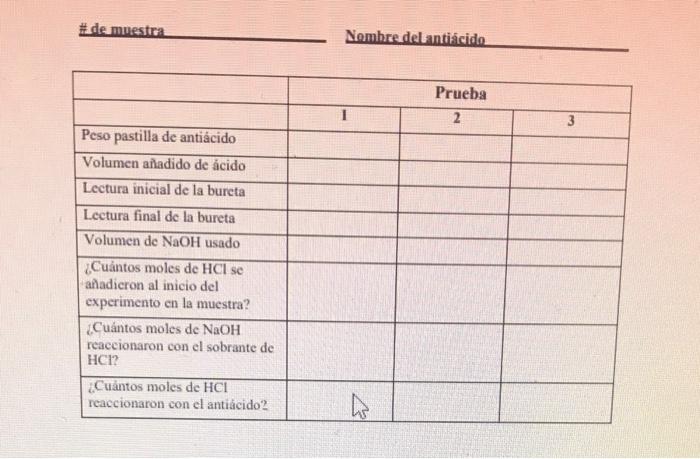
\# de muestra: Nombredelantiścido. \begin{tabular}{|l|l|l|l|} \hline & \multicolumn{2}{|c|}{ Prueba } \\ \hline & I & 2 & \\ \hline Peso pastilla de antiácido & & & \\ \hline Volumen añadido de ácido & & & \\ \hline Lectura inicial de la bureta & & & \\ \hline Lectura final de la bureta & & & \\ \hline Volumen de NaOH usado & & & \\ \hline ¿Cuaˊntos moles de HCl se anadieron al inicio del experimento en la muestra? & & & \\ \hline ¿Cuaˊntos moles de NaOH reaceionaron con el sobrante de HCl? & & & \\ \hline ¿Cuảntos moles de HCl reaccionaron con el antiaˊcido? & & & \\ \hline \end{tabular}
C.N.= ar de antiacido mmoles de H+que reaccionaxon Deferoune la estadistica de la capacidad neumalizante del aniacifo. En el informe incluya: 1. ¿Qué es una titulncióno valoraciòn pđaretroceso? ¿Por qué se utilizan? 2. ¿Qué volumen del HCl que usted aĥadió reaccionafon con el antiácido? Utilizando la Capacidad Neutralizante proenedio que usted obtuvo, responda las preguntas 3 y 4 3. «Caăntos ml de HCl serain nececanos para neutralizar I g de antiàcidoy 4. Si el fabricante de la pastilla que ustedes atilizaron en el experimento recomienda utilizar 2 pastillas cada vez que se tienen los sintomas asumicndo que cada pastilla pesa 1.4gr.cn total. a. LCuintos milimolex de HCT se neutralizarain? b. LCuänos ml del HCl utilizado en el lab se ncutratizariar?. 5. Por que se debe hervir la soluciòn anter de la tialacion'? 6. Como serian los motes de HiCl que resceionan (maborss, rucnores o igualev) a Ia solición no se hicrve? 7. Un antiacido tiene una cipacidad betual izancede 3 milanolos. H. gr. Companaido. 8. Si el aritiacido evia expicito? a. Alectara la precisiàn de aus rexaltados? tabeicent

Estudia mejor, ¡ahora en español!
Entiende todos los problemas con explicaciones al instante y pasos fáciles de aprender de la mano de expertos reales.