Pregunta: PH 1. Al dibujar una curva de titulación, la propiedad que va en el eje de y es y la que va en el eje de x es_odimen de Noora anodicalmo 4. Al titular potenciométricamente una muestra de 0.751 g de un ácido monoprótico desconocido, HA, con NaOH 0.205 M se obtiene la siguiente curva de titulación: 14.00 12.00 10.00 2. En una titulación potenciométrica no es
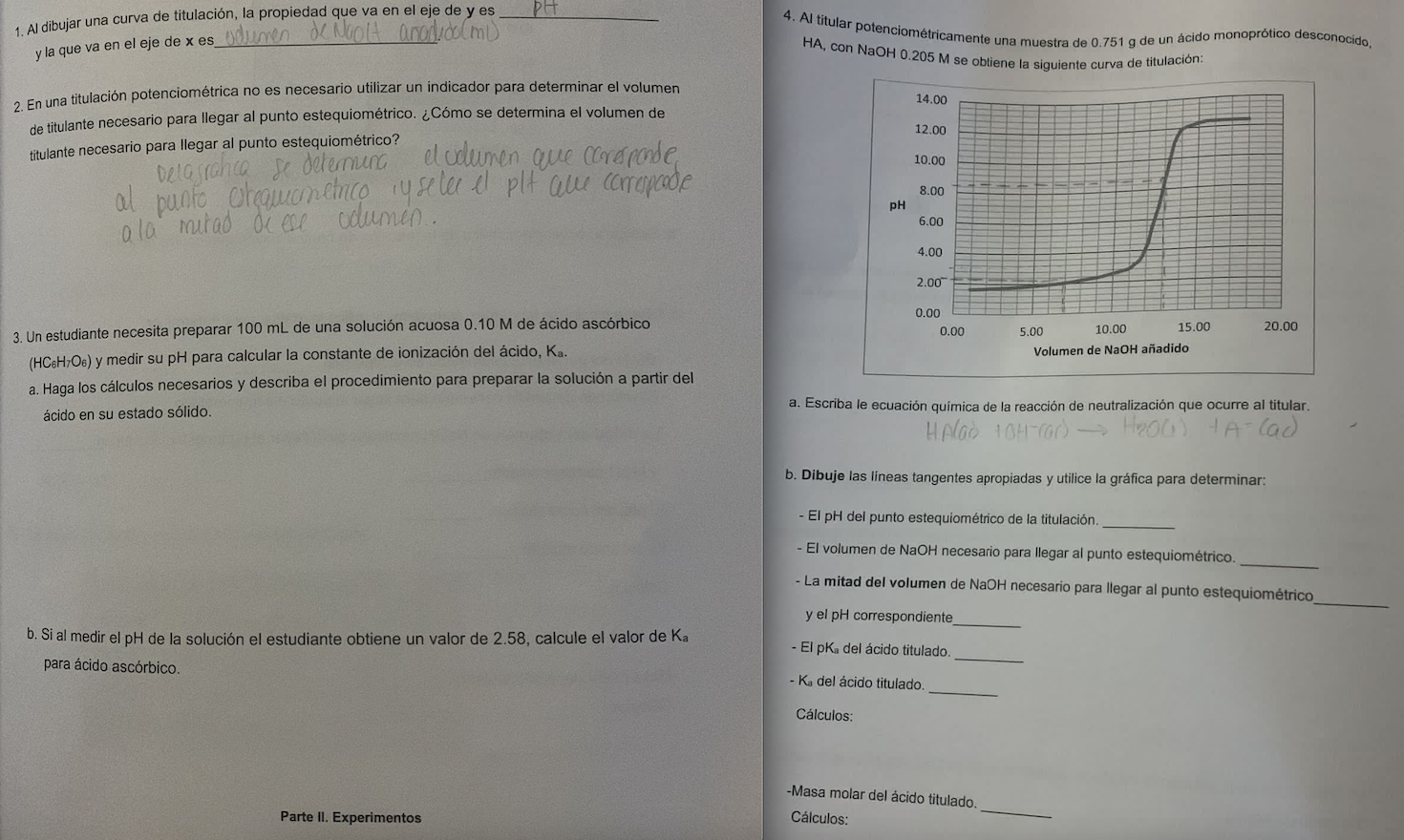
- Esta pregunta aún no se resolvió!¿No es lo que buscas?Envía tu pregunta a un experto en la materia.Texto de la transcripción de la imagen:PH 1. Al dibujar una curva de titulación, la propiedad que va en el eje de y es y la que va en el eje de x es_odimen de Noora anodicalmo 4. Al titular potenciométricamente una muestra de 0.751 g de un ácido monoprótico desconocido, HA, con NaOH 0.205 M se obtiene la siguiente curva de titulación: 14.00 12.00 10.00 2. En una titulación potenciométrica no es necesario utilizar un indicador para determinar el volumen de titulante necesario para llegar al punto estequiométrico. ¿Cómo se determina el volumen de titulante necesario para llegar al punto estequiométrico? Delo sreca se determina el odunen que cresconde al punto Orcauomenico y sellel pl que corrapcode a la mitad de ese odumes. 8.00 pH 6.00 4.00 2.00 0.00 0.00 20.00 5.00 10.00 15.00 Volumen de NaOH añadido 3. Un estudiante necesita preparar 100 mL de una solución acuosa 0.10 M de ácido ascórbico (HC&H:06) y medir su pH para calcular la constante de ionización del ácido, Ka. a. Haga los cálculos necesarios y describa el procedimiento para preparar la solución a partir del ácido en su estado sólido. a. Escriba le ecuación química de la reacción de neutralización que ocurre al titular. HALOd toh-rors - HRoostA-Cad b. Dibuje las líneas tangentes apropiadas y utilice la gráfica para determinar: - El PH del punto estequiométrico de la titulación. El volumen de NaOH necesario para llegar al punto estequiométrico - La mitad del volumen de NaOH necesario para llegar al punto estequiométrico y el pH correspondiente b. Si al medir el pH de la solución el estudiante obtiene un valor de 2.58, calcule el valor de Ka para ácido ascórbico. - El pa del ácido titulado. -K del ácido titulado Cálculos: -Masa molar del ácido titulado. Cálculos: Parte II. Experimentos
Texto de la transcripción de la imagen:
PH 1. Al dibujar una curva de titulación, la propiedad que va en el eje de y es y la que va en el eje de x es_odimen de Noora anodicalmo 4. Al titular potenciométricamente una muestra de 0.751 g de un ácido monoprótico desconocido, HA, con NaOH 0.205 M se obtiene la siguiente curva de titulación: 14.00 12.00 10.00 2. En una titulación potenciométrica no es necesario utilizar un indicador para determinar el volumen de titulante necesario para llegar al punto estequiométrico. ¿Cómo se determina el volumen de titulante necesario para llegar al punto estequiométrico? Delo sreca se determina el odunen que cresconde al punto Orcauomenico y sellel pl que corrapcode a la mitad de ese odumes. 8.00 pH 6.00 4.00 2.00 0.00 0.00 20.00 5.00 10.00 15.00 Volumen de NaOH añadido 3. Un estudiante necesita preparar 100 mL de una solución acuosa 0.10 M de ácido ascórbico (HC&H:06) y medir su pH para calcular la constante de ionización del ácido, Ka. a. Haga los cálculos necesarios y describa el procedimiento para preparar la solución a partir del ácido en su estado sólido. a. Escriba le ecuación química de la reacción de neutralización que ocurre al titular. HALOd toh-rors - HRoostA-Cad b. Dibuje las líneas tangentes apropiadas y utilice la gráfica para determinar: - El PH del punto estequiométrico de la titulación. El volumen de NaOH necesario para llegar al punto estequiométrico - La mitad del volumen de NaOH necesario para llegar al punto estequiométrico y el pH correspondiente b. Si al medir el pH de la solución el estudiante obtiene un valor de 2.58, calcule el valor de Ka para ácido ascórbico. - El pa del ácido titulado. -K del ácido titulado Cálculos: -Masa molar del ácido titulado. Cálculos: Parte II. Experimentos

Estudia mejor, ¡ahora en español!
Entiende todos los problemas con explicaciones al instante y pasos fáciles de aprender de la mano de expertos reales.