¡Tu solución está lista!
Nuestra ayuda de expertos desglosó tu problema en una solución confiable y fácil de entender.
Mira la respuestaMira la respuesta done loadingPregunta: Átomo de Hidrógeno (a) Encuentre (r) y (r2) para un electrón en el estado fundamental del átomo de Hidrógeno. Exprese su respuesta en términos del radio de Bohr. (b) Encuentre (x) y (r2) para un electrón en el estado fundamental del átomo de Hidrógeno. Comparelo con el resultado anterior. (c) Encuentre (x²) en el estado n = 2, l = 1, m = 1.* *Sea ao = ²/pe²

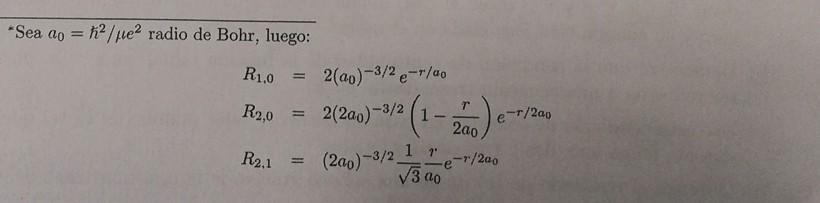
Image translation:
a, b) Find expected value of r, r^2, x and x^2. For an electron in the ground state of the hydrogen atom. Express your answer in terms of the Bohr radius.
C) find the expected value of x^2 for the states n= 2,l=1,m=1 More details see image
- Esta es la mejor manera de resolver el problema.Solución100% (2 calificaciones)
Texto de la transcripción de la imagen:
Átomo de Hidrógeno (a) Encuentre (r) y (r2) para un electrón en el estado fundamental del átomo de Hidrógeno. Exprese su respuesta en términos del radio de Bohr. (b) Encuentre (x) y (r2) para un electrón en el estado fundamental del átomo de Hidrógeno. Comparelo con el resultado anterior. (c) Encuentre (x²) en el estado n = 2, l = 1, m = 1.*
*Sea ao = ²/pe² radio de Bohr, luego: R1.0 R2,0 R2,1 = 2(ao)-3/2 e-r/ao = 2(200)-3/2 (1-2) 6-1/20 1 r (200)-3/2_ -r/200 √3.00

Estudia mejor, ¡ahora en español!
Entiende todos los problemas con explicaciones al instante y pasos fáciles de aprender de la mano de expertos reales.
