¡Tu solución está lista!
Nuestra ayuda de expertos desglosó tu problema en una solución confiable y fácil de entender.
Mira la respuestaMira la respuesta done loadingPregunta: When heated to a constant temperature, 800 ° C, different starting mixtures of CO, H20, CO2 and H2 react to achieve compositions that adhere to the same equilibrium (the value of Q changes until it is equal to the value of Kc). The Kc value is 0.64, the equilibrium constant for the reaction in these conditions.Here are the initial concentrations of reagents
When heated to a constant temperature, 800 ° C, different starting mixtures of CO, H20, CO2 and H2 react to achieve compositions that adhere to the same equilibrium (the value of Q changes until it is equal to the value of Kc). The Kc value is 0.64, the equilibrium constant for the reaction in these conditions.Here are the initial concentrations of reagents and products for three experiments that include this reaction. Determine in which direction the reaction advances as it progresses towards equilibrium in each of the three experiments shown.- Hay 4 pasos para resolver este problema.SoluciónPaso 1Mira la respuesta completa
Para resolver este ejercicio hay que utilizar el concepto de "cociente de reacción (Qc)" y correspon...
Paso 2 DesbloqueaPaso 3DesbloqueaPaso 4DesbloqueaRespuestaDesbloquea
DesbloqueaPaso 3DesbloqueaPaso 4DesbloqueaRespuestaDesbloquea
Texto de la transcripción de la imagen:
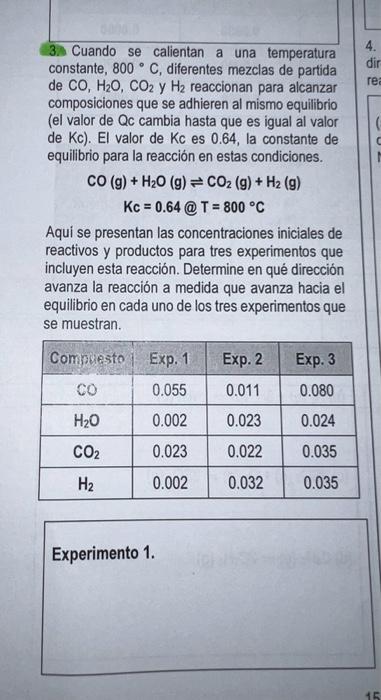
3. Cuando se calientan a una temperatura constante, 800∘C, diferentes mezclas de partida de CO,H2O,CO2 y H2 reaccionan para alcanzar composiciones que se adhieren al mismo equilibrio (el valor de Qc cambia hasta que es igual al valor de Kc ). EI valor de Kc es 0.64 , la constante de equilibrio para la reacción en estas condiciones. CO(g)+H2O(g)⇌CO2( g)+H2( g)Kc=0.64@ T=800∘C Aqui se presentan las concentraciones iniciales de reactivos y productos para tres experimentos que incluyen esta reacción. Determine en qué dirección avanza la reacción a medida que avanza hacia el equilibrio en cada uno de los tres experimentos que se muestran.
2] =0.90

Estudia mejor, ¡ahora en español!
Entiende todos los problemas con explicaciones al instante y pasos fáciles de aprender de la mano de expertos reales.