¡Tu solución está lista!
Nuestra ayuda de expertos desglosó tu problema en una solución confiable y fácil de entender.
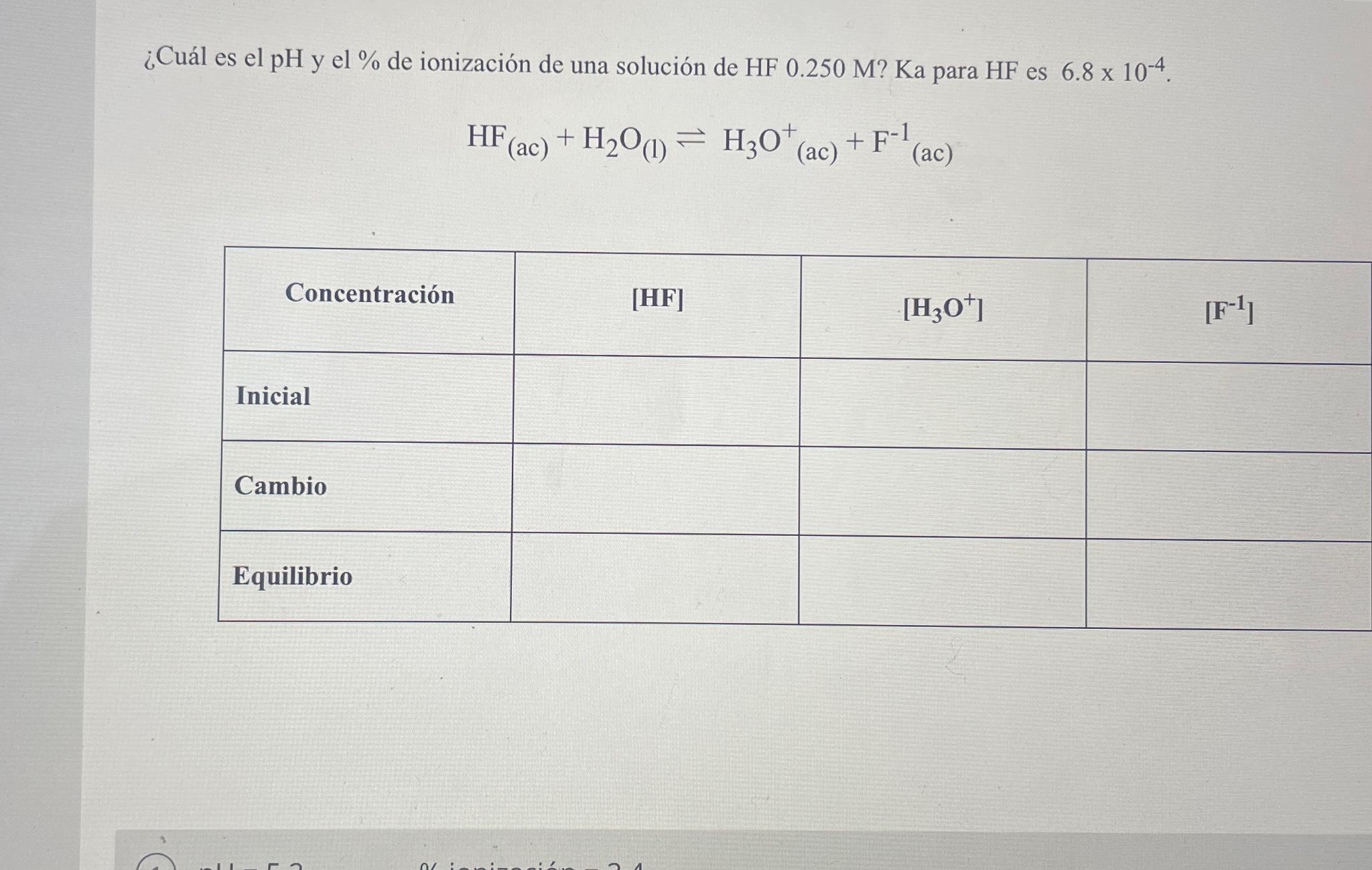
Mira la respuestaMira la respuesta done loadingPregunta: ¿Cuál es el pH y el % de ionización de una solución de HF 0.250 M? Ka para HF es 6.8×10-4.HF(ac)+H2O(l)⇌H3O(ac)++F(ac)-1\table[[Concentración,HF,H3O+,F-1
Cul es el pH y el de ionizacin de una solucin de HF M Ka para HF estableConcentracin- Hay 2 pasos para resolver este problema.Solución

Estudia mejor, ¡ahora en español!
Entiende todos los problemas con explicaciones al instante y pasos fáciles de aprender de la mano de expertos reales.