¡Tu solución está lista!
Nuestra ayuda de expertos desglosó tu problema en una solución confiable y fácil de entender.
Mira la respuestaMira la respuesta done loadingPregunta: A continuación, se presenta una reacción de oxidación-reducción en medio ácido: 312(s) + 5C103 (ac) + 3H20 (1) ► 6103 → +501(ac) + 6H* (ac) (ac) Eento que se reduce es: Select one: O a. H O b. CI Ос. О O d. 1 El pH de una solución 0.1 M de NH3 es 11.13. La reacción en equilibrio es el siguiente: NH3 (ac) + H20 (1) + NH4 + OH(ac) (ac) Cel Kb. Select one: O
- Esta es la mejor manera de resolver el problema.SoluciónTe mostramos cómo abordar esta pregunta.
Este consejo generado con IA está basado en la solución completa de Chegg. ¡Regístrate para ver más!
To determine which element is reduced in the given redox reaction, identify the changes in oxidation numbers for each element involved in the reactants and products.

Texto de la transcripción de la imagen:
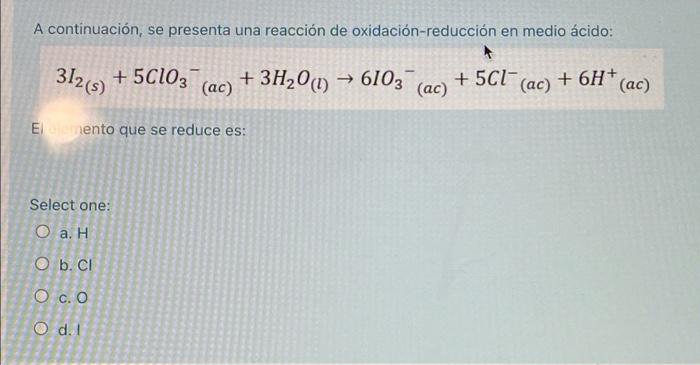
A continuación, se presenta una reacción de oxidación-reducción en medio ácido: 312(s) + 5C103 (ac) + 3H20 (1) ► 6103 → +501(ac) + 6H* (ac) (ac) Eento que se reduce es: Select one: O a. H O b. CI Ос. О O d. 1
El pH de una solución 0.1 M de NH3 es 11.13. La reacción en equilibrio es el siguiente: NH3 (ac) + H20 (1) + NH4 + OH(ac) (ac) Cel Kb. Select one: O a. 3.2 x 10-5 O b.4.5 x 10-4 O c. 1.8 x 10-5 O d. 2.0 x 10-4
A continuación, se presenta una reacción de oxidación-reducción: Zn(s) + Cu+2 (ac) – Zn+2 Zn+2 (ac) + Cu(s) ( valuar la reacción química presentada, podemos decir que: Select one: O a. Cu+2 es el que se reduce, es el agente oxidante O b. Todas las opciones son correctas O c. La oxidación y reducción de los reactivos ocurre simultáneamente O d. Zn es el que se oxida, es el agente reductor

Estudia mejor, ¡ahora en español!
Entiende todos los problemas con explicaciones al instante y pasos fáciles de aprender de la mano de expertos reales.