¡Tu solución está lista!
Nuestra ayuda de expertos desglosó tu problema en una solución confiable y fácil de entender.
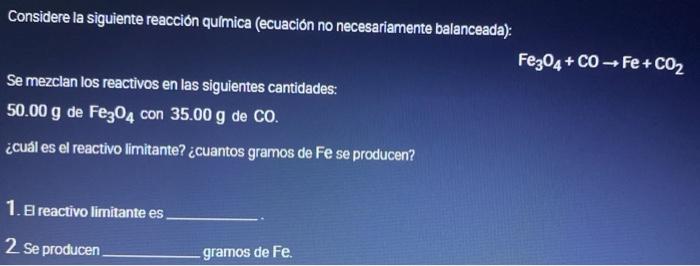
Mira la respuestaMira la respuesta done loadingPregunta: Considere la siguiente reacción química (ecuación no necesariamente balanceada): Se mezclan los reactivos en las siguientes cantidades: 50.00 g de Fe304 con 35.00 g de CO. ¿cuál es el reactivo limitante? ¿cuantos gramos de Fe se producen? 1. El reactivo limitante es 2 Se producen - gramos de Fe. Fe3O4 + CO→Fe + CO₂
- Esta es la mejor manera de resolver el problema.Solución
Please follow the below-…
Mira la respuesta completa
Texto de la transcripción de la imagen:
Considere la siguiente reacción química (ecuación no necesariamente balanceada): Se mezclan los reactivos en las siguientes cantidades: 50.00 g de Fe304 con 35.00 g de CO. ¿cuál es el reactivo limitante? ¿cuantos gramos de Fe se producen? 1. El reactivo limitante es 2 Se producen - gramos de Fe. Fe3O4 + CO→Fe + CO₂

Estudia mejor, ¡ahora en español!
Entiende todos los problemas con explicaciones al instante y pasos fáciles de aprender de la mano de expertos reales.