¡Tu solución está lista!
Nuestra ayuda de expertos desglosó tu problema en una solución confiable y fácil de entender.
Mira la respuestaMira la respuesta done loadingPregunta: Con los siguientes datos debo calcular el Ka experimental. El Ka teórico es 1.75 x 10^-5 (ácido acético).Luego debo completar la segunda tabla utilizando los datos de la Titulación.
Con los siguientes datos debo calcular el Ka experimental. El Ka teórico es 1.75 x 10^-5 (ácido acético).Luego debo completar la segunda tabla utilizando los datos de la Titulación.
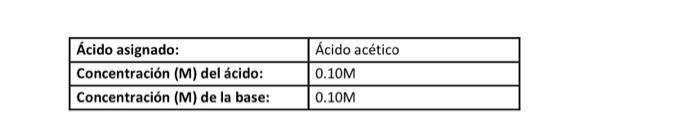
Aqui esta la concentracion de la base y de el ácido. La base utilizada es NaOH.solo falta calcular el porcentaje de error en la tabla.
- Intenta enfocarte en un paso a la vez. ¡Tú puedes!SoluciónPaso 1Mira la respuesta completa
En el punto de semi equivalencia (punto medio de neutralización), la cantidad del ácido y báse conj...
Paso 2 DesbloqueaPaso 3DesbloqueaPaso 4DesbloqueaPaso 5DesbloqueaRespuestaDesbloquea
DesbloqueaPaso 3DesbloqueaPaso 4DesbloqueaPaso 5DesbloqueaRespuestaDesbloquea
Texto de la transcripción de la imagen:
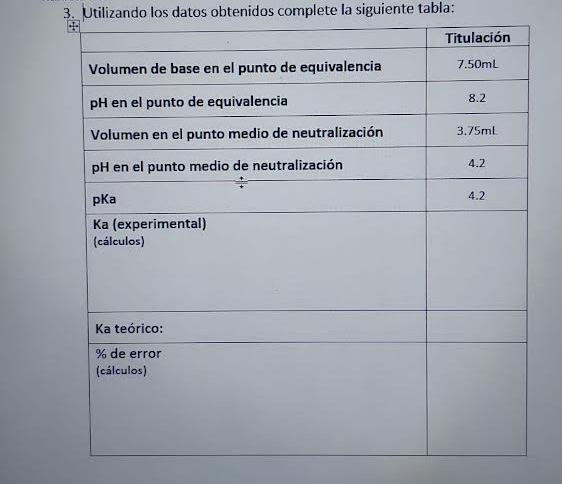
3. Utilizando los datos obtenidos complete la siguiente tabla: \begin{tabular}{|l|c|} \hline & Titulación \\ \hline Volumen de base en el punto de equivalencia & 7.50 mL \\ \hline pH en el punto de equivalencia & 8.2 \\ \hline Volumen en el punto medio de neutralización & 3.75 mL \\ \hline pH en el punto medio de neutralización & 4.2 \\ \hline pKa & 4.2 \\ \hline Ka (experimental) (caˊlculos) & \\ \hline Ka teórico: & \\ \hline (cálculos) \end{tabular}
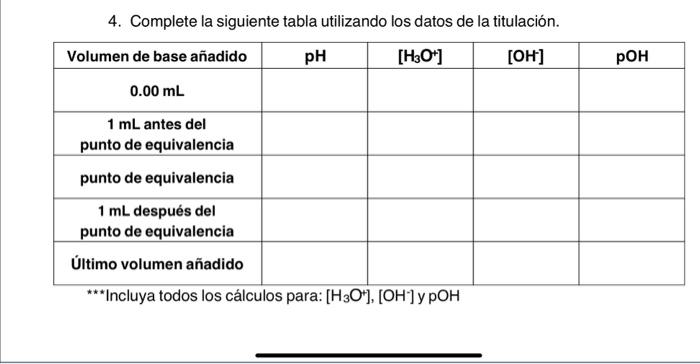
4. Complete la siguiente tabla utilizando los datos de la titulación. *** Incluya todos los cálculos para: [H3O+],[OH−]y pOH
\begin{tabular}{|l|l|} \hline Ácido asignado: & Ácido acético \\ \hline Concentración (M) del ácido: & 0.10M \\ \hline Concentración (M) de la base: & 0.10M \\ \hline \end{tabular}
3. Utilizando los datos obtenidos complete la siguiente tabla:

Estudia mejor, ¡ahora en español!
Entiende todos los problemas con explicaciones al instante y pasos fáciles de aprender de la mano de expertos reales.