Chemistry Archive: Questions from April 08, 2022
-
Give the product of each reaction, include stereochemistry where applicable.
Provea et producto de cada reacción, incluya estereoquímica cuando aplique. HO роо, но те 2) CH Hyh CH MCPELA 10 CH 11 DO 2) Na 12 110, 23. HO KM HO1 answer -
allaven -orla 7. CH3 Retroanálisis: Síntesis: (alquilación , hidrólisis del éster, descarboxilación)1 answer -
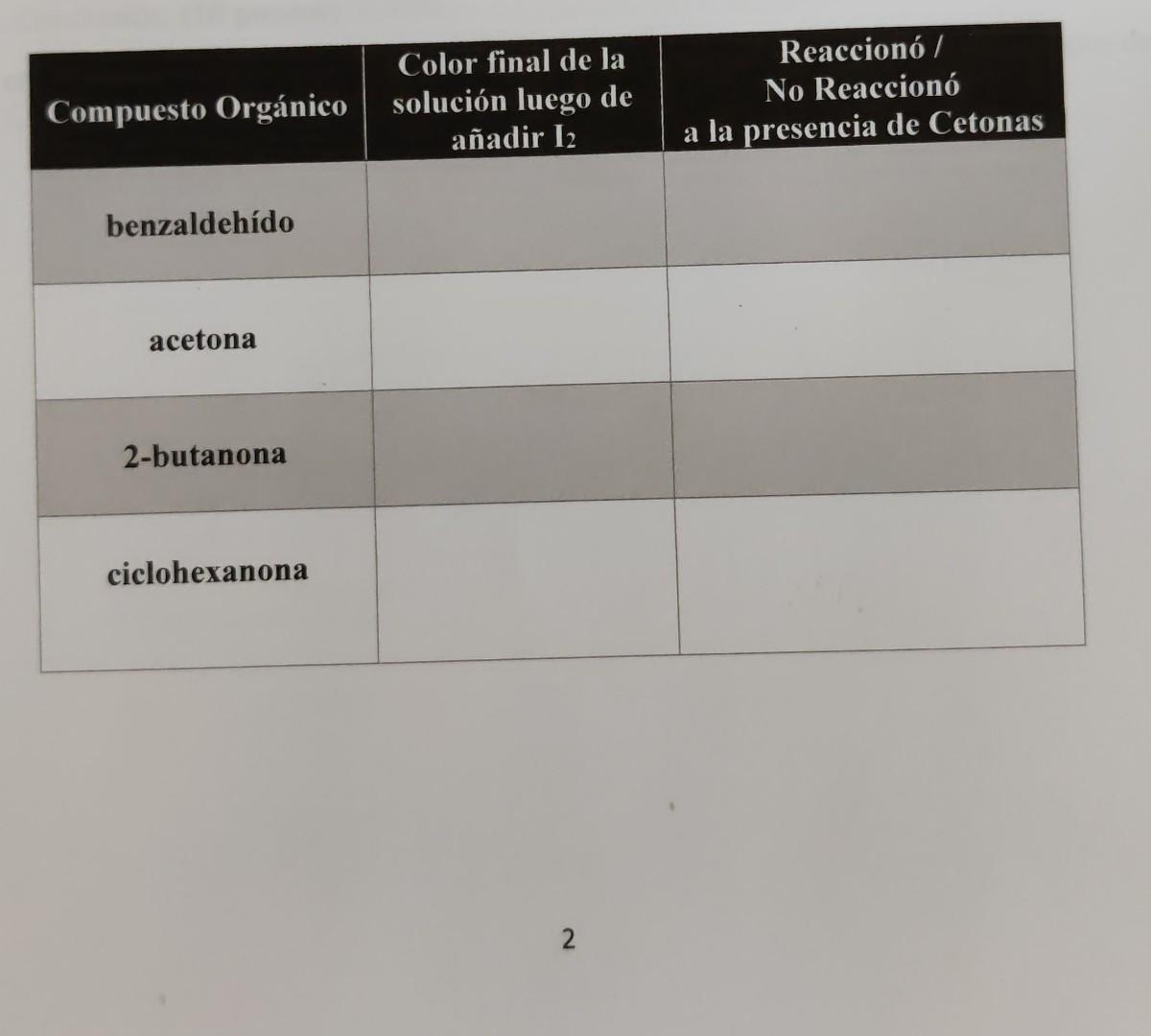
Compuesto Orgánico Color final de la solución luego de añadir 12 Reaccionó / No Reaccionó a la presencia de Cetonas benzaldehído acetona 2-butanona ciclohexanona 21 answer -
El valor de AH para la siguiente reacción es -790 kJ. Calcule el cambio en entalpia, en kl, para la reacción de 2.85g de S según la siguiente reacción: 25 (s) + O2(g) AHN - 790kJ *Coloque solament1 answer -
1 answer
-
Analyze the IR spectra of cyclohexanol and cyclohexene. Mark the signals (bands) that confirm its functionalities.
FTIR Common Name: Cyclohexene IUPAC Name: Cyclohexene BP: 83 MP: -104 MICRORS 1.00 22 23 24 25 26 2722222 SE 55 11 13 12 13 14 15 16 17 181221222 10.0 . M 0.1 リード 8 8 8 2233899 RAZNOVO 30 20 101 answer -
1 answer
-
For the reaction shown, calculate how many moles of NO2 are formed when 12.90 g of N2O5 reacts completely. Molecular Weight: N2O5: 108.02 g/mol NO2: 46.01 g/mol O2: 32.00 g/mol 2 N2O5(g) → 4 NO
Para la reacción que se muestra, calcule cuántos moles de NO2 se forman cuando 12.90 g de N205 reacciona por completo. Peso moleculares: N205: 108.02 g/mol NO2: 46.01 g/mol O2: 32.00 g/mol 2 N205(9)1 answer -
For the reaction shown, calculate the percent yield of the production of 20.23 g NO2 formed when 27.90 g N2O5 is completely reacted. 2 N2O5(g) → 4 NO2(g) + O2(g) Molecular Weight: N2O5: 108.02 g/
4 points Save Answer Para la reacción que se muestra, calcule el porciento de rendimiento de la produccion de 20.23 9 NO2 formados cuando 27.90 g de N205 reacciona por completo. 2 N205(9) — 4 NO2(g1 answer -
For the reaction shown, calculate how many moles of O2 are formed when 1.8 mol N2O5 reacts completely. Molecular Weight: N2O5: 108.02 g/mol NO2: 46.01 g/mol O2: 32.00 g/mol
Para la reacción que se muestra, calcule cuántos moles de O2 se forman cuando 1.8 mol N205 reacciona por completo. Peso moleculares: N205: 108.02 g/mol NO2: 46.01 g/mol 02:32.00 g/mol 2 N205(9) - 41 answer -
Predict the major product of the following Claisen condensation. لہ OEL 1. NaOEt EtOH 2. H2O, H* ? ہ Et عد لہ en lezen OE Et OE Et b C d1 answer -
1 answer
-
¿Cuál es la temperatura final (°C) en cuando 15 g de Hg que están a 22.0°C reciben 43.81 de calor? (calor especifico de Hg = 0.139) * Colocar solo en valor numerico. What is the final temperatu1 answer -
Una de 25 de 12 calorimetro de bomba con una cidade de care 580 tatoertura del contra de 20.30 u seria el calor de combine 12 en molt0 answers -
1 answer
-
¿Cuáles serán los productos para la siguiente reaccion? Mgs (ac) + CuCl2 (ac) a. MgCl(a) y Cu2$ (ac) Ob. CuS() M92Cl(ac) c. Cus (s) MgCl2 (ac) Od. No forma ningun producto1 answer -
na mestra de 4.758 de CH12 Sequera en un calorimetro de bomba con una capacidad total de calor de 5.86 C Latentura decimetro aumenta de 23.5*0 a 39.8°C Cuál seria el calor de combustión de C8H12 en1 answer -
Un procedimiento en el laboratorio sugiere preparar 400.0mL de una solución 1.50M de NaNO3. ¿Cuál es la masa (eng) necesaria de NaNO3 para preparar la solución? *Coloque solamente el valor numeric1 answer -
El valor de AH para la siguiente reacción es - 790 kl. Calcule el cambio en entalpia, en kl, para la reacción de 2.85g de S según la siguiente reacción: 28 (s) + O2(g) - 2 SO3 (a) ΔΗ= - 790KJ *C1 answer -
English translation: What is the concentration of hydroxide ions in pure water at 30°C if Kw at this temperature is 1.47 x 10^-14?
¿Cuál es la concentración de iones de hidróxido en agua pura a 30°C si Kw a esta temperatura es 1.47 x 10-14? a. 1.00 x 10-7M b. 8.93 x 10-8 M O c. 1.21 x 10-7M O d. 1.30 x 10-7 M e. 1.47 x 10-7M1 answer -
Which of the following are NOT a conjugate pair?
¿Cuáles de los siguientes NO constituyen un par conjugado? O a. C2H302 / HC2H302 a Ob O b. H2SO3 / HSO3 O c. NH4+ / NH3 O d. H30+ / OH O e. H3PO4 / H2PO4"1 answer -
Determine the Ka for an acid that is 0.500 M in a solution that has a pH of 3.77?
Determine la ka para un ácido que es 0.500 M en una solución que tiene pH de 3.77. O a. 1.16 x 10-7 O b. 2.89 x 10-8 c. 5.77 x 10-8 O d. 3.62 x 10-7 e. 1.70 x 10-31 answer -
Identifique cuales de los siguientes compuestos son bases: Ca(OH)2, KOH, H2C204 y HI. a. H2C204 y HD O b.Ca(OH)2 y KOH c. Solamente KOH d. Solamente HI1 answer -
The correct expression of the equilibrium constant that applies to hydrolisis for the KCN salt is:
La expresión correcta de la constante de equilibrio que aplica a la hidrólisis para la sal KCN es: a. K = [K+] (CN) O b. K = ([H3O+] (CN-])/(HCN) O c. K = ([OH) [HCN])/(CN) O d. K = [HCN]/([H3O+] (C1 answer -
Determine el rendimiento teorico del HCI 6173.0g de Biz y 48.59 de H20 reaccionan segun la sigueinte ecuacion Hзвоз (s) • Знсi ta) BC13 (9) 3H201 answer -
En la siguiente reacción. ¿cual de los elementos es el agente reductor? Zn(s) + 2AGNO3 (ac) - Zn(NO3)2 (ac) + 2AG (s) DaN b. Ag Oco .1 answer


