Chemistry Archive: Questions from April 01, 2022
-
1 answer
-
1. ¿Cuáles son la concentración de ion hidronio y la y concentración de ion hidróxido en agua pura a 80 °C? El valor de Kw para agua a 80 °C es 2.4 x 10-13.1 answer -
2. Escribe ecuaciones separadas que representan reacción de H2PO4-1 (a) como un ácido con OH-1 (b) como base con HCI (a) como un ácido con OH-1 (b) como base con HCI1 answer -
3. La concentración de vinagre en el ion hidronio es de aproximadamente 4 x 10-3 M. ¿Cuáles son los valores correspondientes de pOH y pH?1 answer -
4. Provea una síntesis alterna (diferente a la que hicieron en este experimento) para sintetizar cada uno de los productos 1-fenil-1-propanol y 2-fenil-2-propanol.1 answer -
A 25 °C, la solubilidad del NaCl es de 36 g/100 ml agua. ¿Qué pasa cuando se añaden 70 g de NaCl a 1L de agua? O a la solución es insaturada y se disuelve la totalidad del NaCl O b. cristaliza la1 answer -
translation: If a compound has an enthalpy of fusion of 4.9kJ/mol and an enthalpy of sublimation of 38.6kJ/mol, its enthalpy of vaporization is __kJ/mol.
Tiempo restant Si un compuesto tiene una entalpia de fusión de 49 ki/mol y una entalpla de sublimacion de 38,6 l/mol su entalpia de vaporizadones de Il/mol Da-33.7 Ob ninguna respuesta es la correcta1 answer -
translation: consider the following H2 combustion: 2H2(g) + O2(g) = 2H2O(g) If hydrogen burns at a rate of x M/s, the rate of oxygen consumption is ____ m/s.
Considere la combustión de Ha siguiente: 2H2(g) + O2(g) ----> 2H2O(g) - Si el hidrógeno se quema a una velocidad dex M/s, la velocidad de consumo del oxígeno es de m/s: O a. 4x O b. 0.25 x O c.0.51 answer -
Considere la siguiente gráfica de la concentración de una sustancia contra tiempo. ¿Cuál(es) de la siguientes aclaraciones acerca de la reacción es/son cierta(s)? 3 [x] 2 1 Tiempo a. la velocidad1 answer -
¿Cuál de las siguientes aclaraciones es falsa? O a. Las solubilidades de los gases en agua disminuyen cuando la temperatura aumenta O b. Las solubilidades de los solutos sólidos en agua aumenta con1 answer -
Pick the main product of the reaction
Pregunta 5 Escoja el producto principal de la siguiente secuencias de reacciones: Incorrecta Осн. Se puntúa 0.0 sobre 2.0 PBry NaSH DMSO P Marcar pregunta ÕH O a. HS SH b. X OCH SH C. SH SH d. О1 answer -
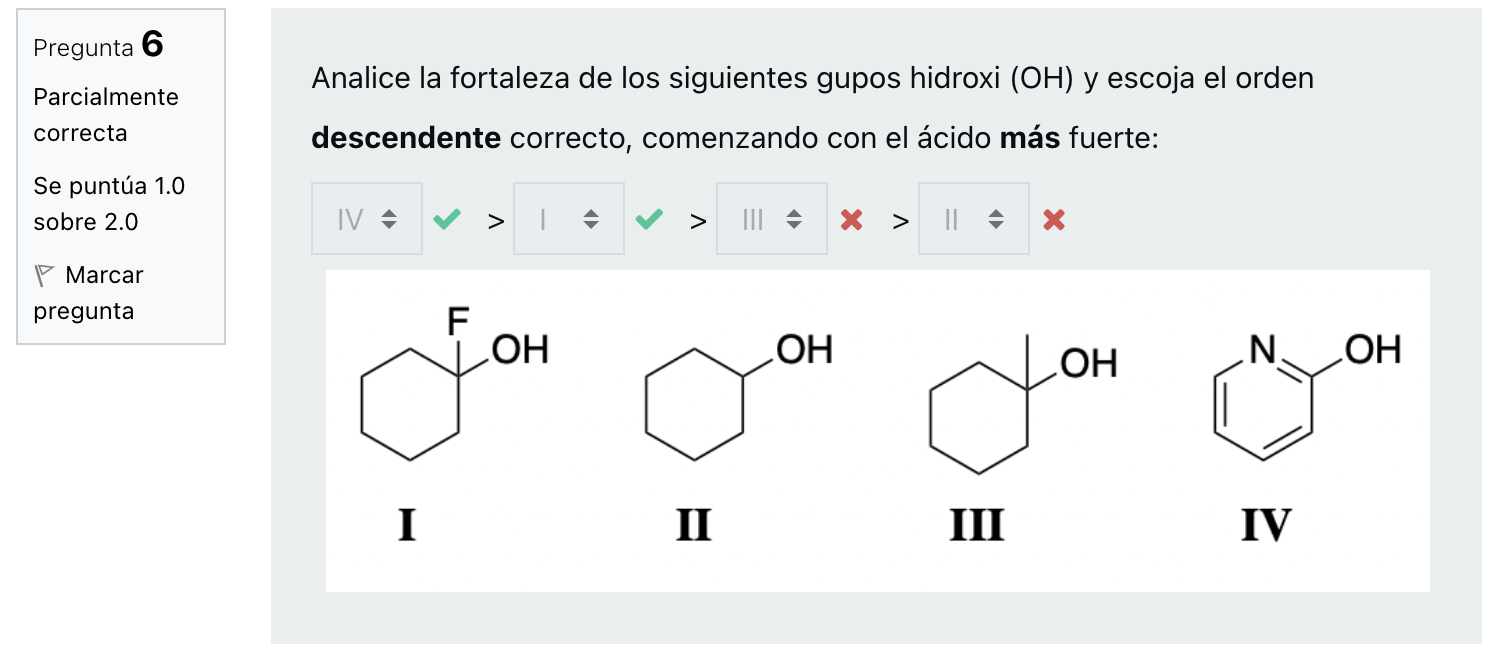
Pregunta 6 Parcialmente Analice la fortaleza de los siguientes gupos hidroxi (OH) y escoja el orden descendente correcto, comenzando con el ácido más fuerte: correcta Se puntúa 1.0 sobre 2.0 IV > >1 answer -
1 answer
-
1 answer
-
1 answer
-
1 answer
-
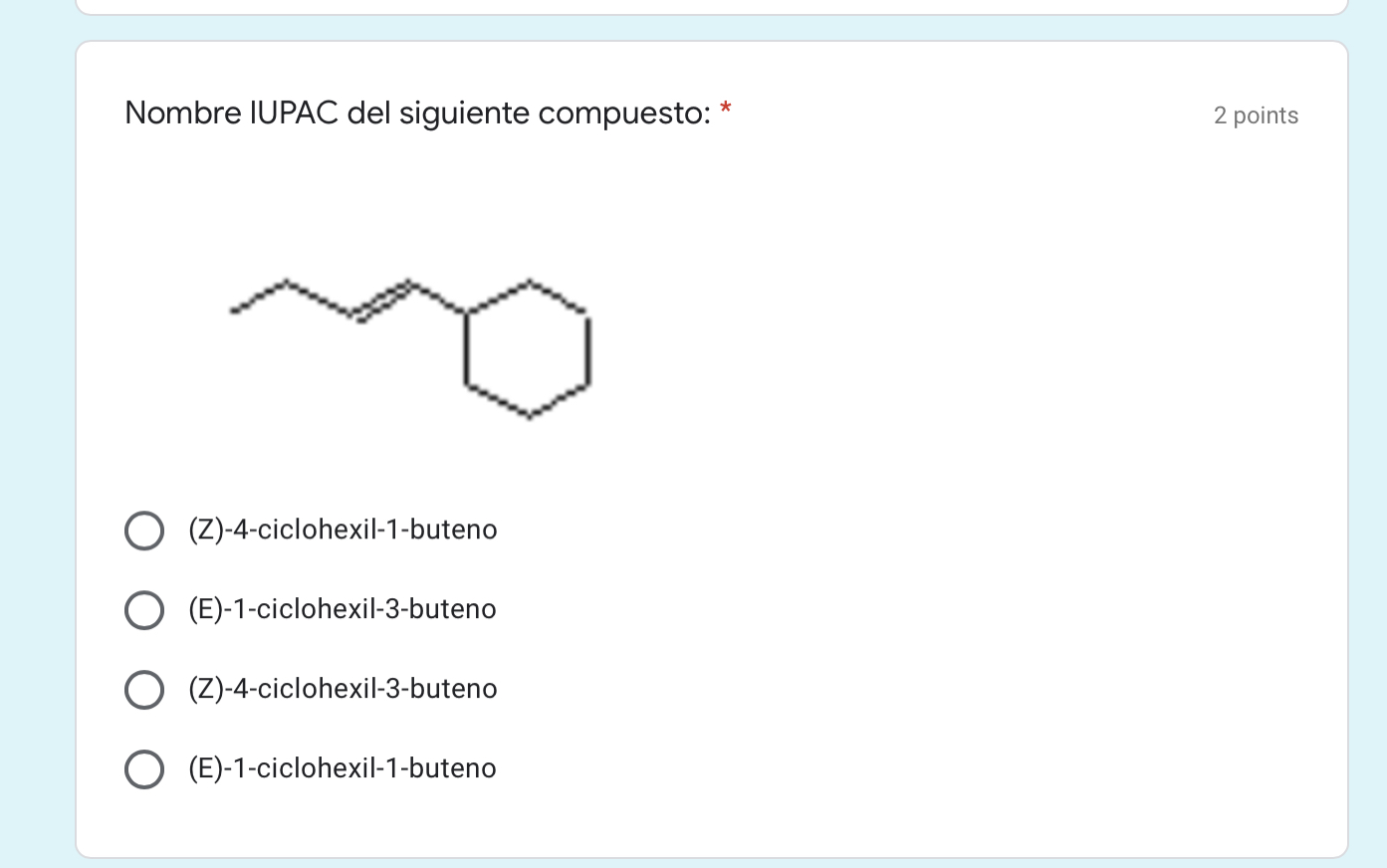
Nombre IUPAC del siguiente compuesto: * 2 points (Z)-4-ciclohexil-1-buteno (E)-1-ciclohexil-3-buteno (Z)-4-ciclohexil-3-buteno (E)-1-ciclohexil-1-buteno1 answer -
2 points ¿Cuál de los siguientes forma el carbocation mas estable cuando reacciona con HBr? * 3-metil-2-hexeno 5,5-dimetil-2-hexeno 5-metil-2-hexeno 1-hexeno 4-metil-2-hexeno1 answer -
2 points ¿Cuál es el producto mayoritario de la reacción de HBr con 3-metil-1- buteno? Para obtener crédito, tiene que marcar todas las respuestas correctas única y exclusivamente. * у CH3CH2CH21 answer -
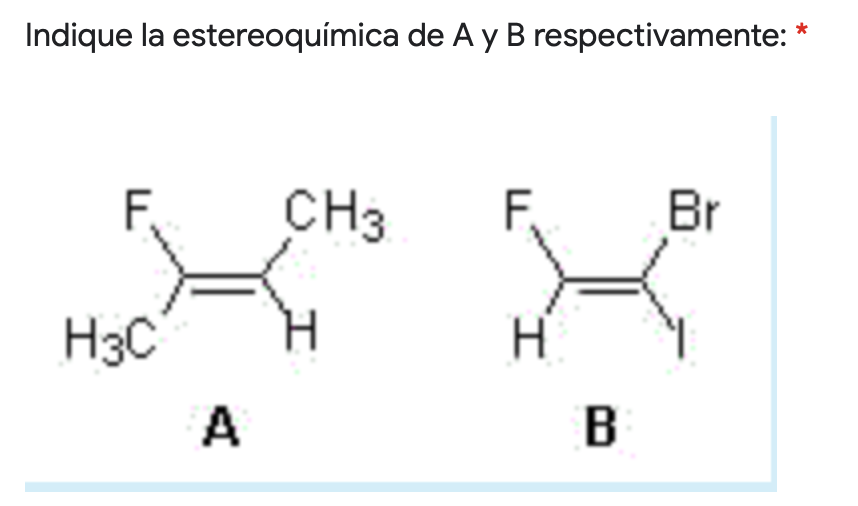
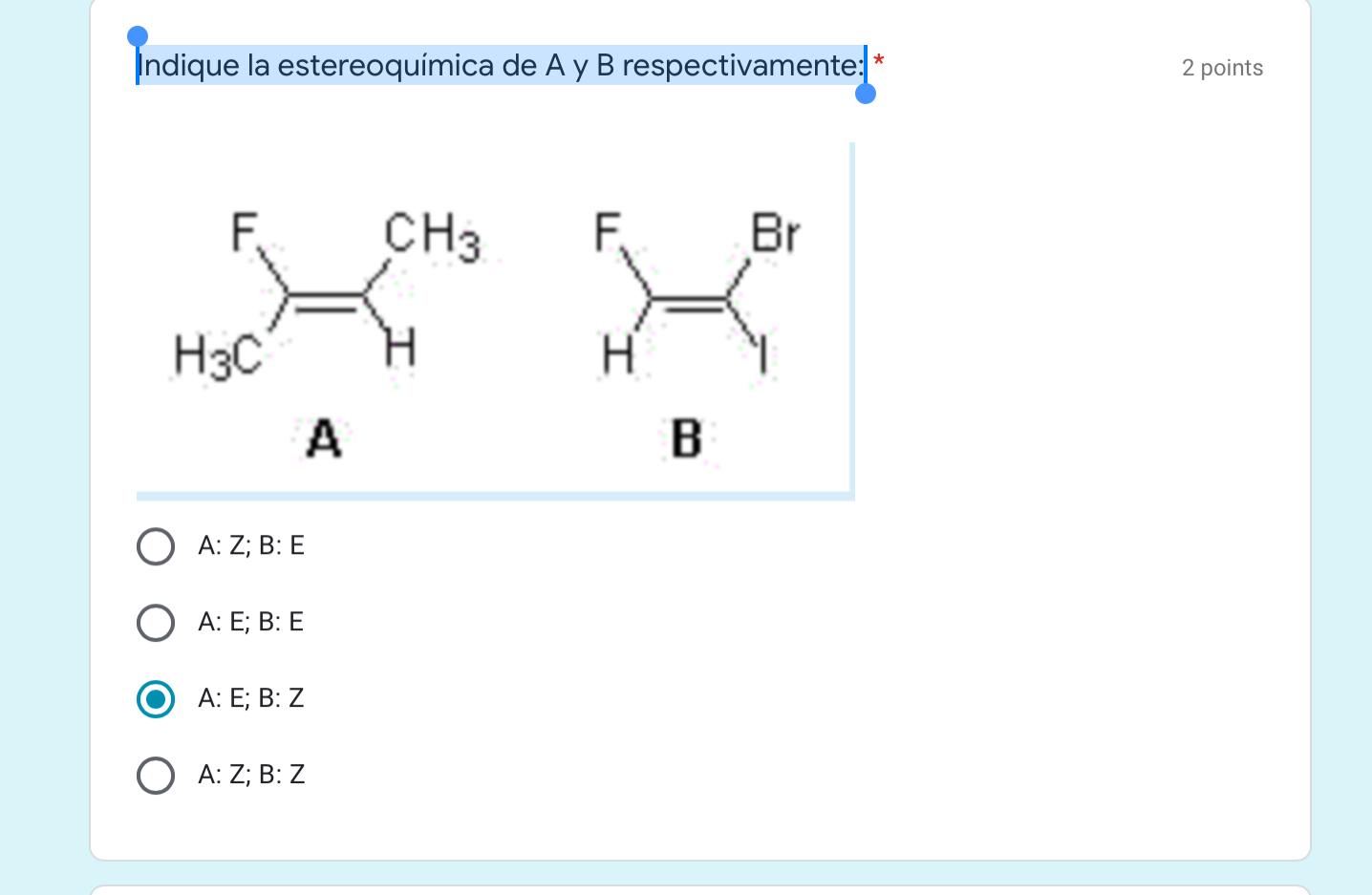
ndique la estereoquímica de A y B respectivamente: * y 2 points CH3 F Br H3C H A В B A: Z; B: E A: E; B: E A: E; B: Z A: Z; B: Z1 answer -
1 answer
-
Morphine (C17H19O3N) (MM 285.34) is a weak base with a Kb of 7.4 x 10-7. Calculate the pH of a solution containing a concentration of morphine of 1.75 x 10-4 M. C17H19O3N(aq) + H2O(l) ⇌ OH-(aq) + C1
(8 ptos.) La morfina (C17H1903N) (MM 285.34) es una base débil con un Ko de 7.4 x 10-7. Calcule el pH de una solución que contiene una concentración de morfina de 1.75 x 10-4 M. C17H1903N(ac) + H2O1 answer -
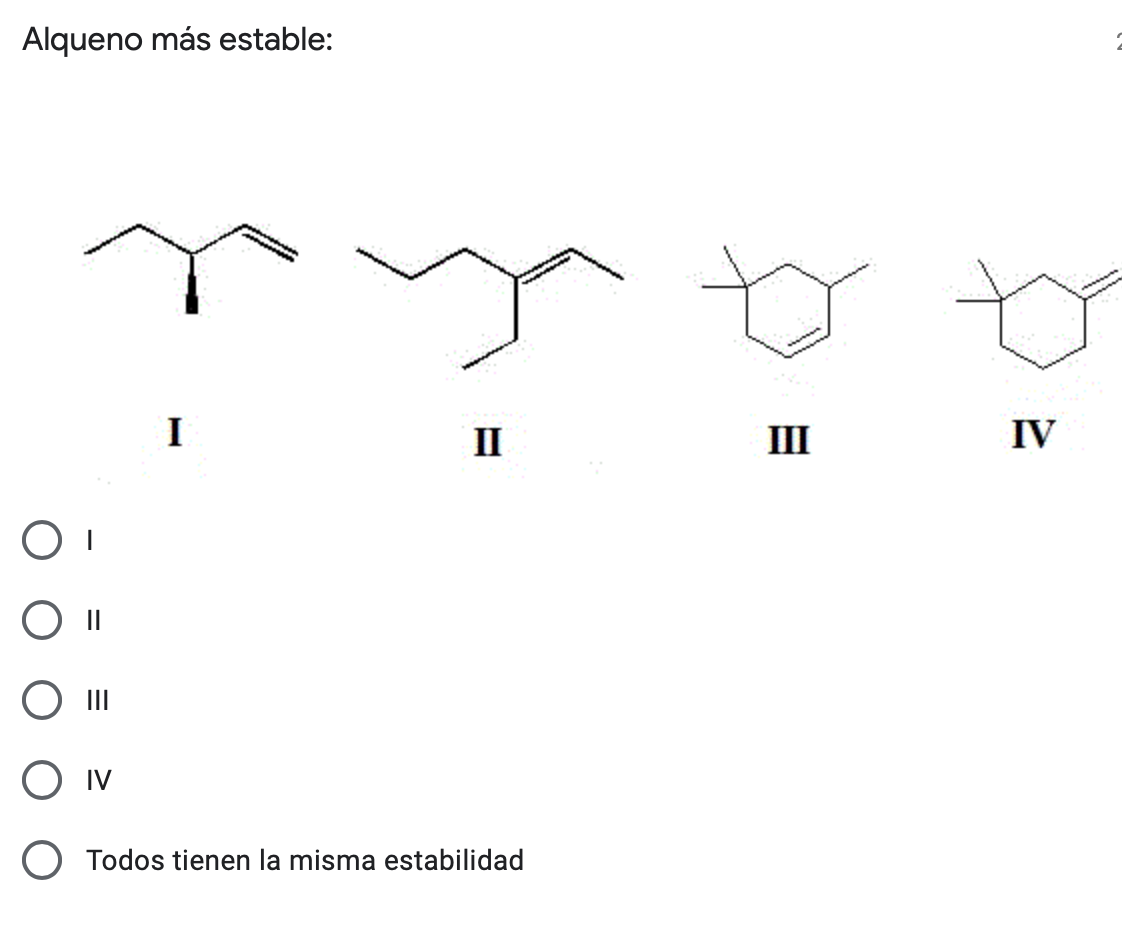
Alqueno más estable trans-2-hexeno 1-metilciclohexeno 4-metilciclohexeno 3-metilciclohexeno 1-hexeno1 answer
-
Kp has a value of 1.85. Calculate the value of Kc
4. (3 ptos.) Para la siguiente reacción: SO2(g) +0200) - S03(6) + A 1000K, Kp tiene un valor de 1.85. Calcule el valor de Ka.1 answer -
1 answer
-
A 0.10 M solution of a weak monoprotic acid (HA) has a pH of 2.39. HA(aq) + H2O(l) ⇌ H3O+ (aq) + A-(aq) What is the value of its acid dissociation constant, Ka?
Una solución 0.10 M de un ácido débil monoprótico (HA) tiene un pH de 2.39. HA(ac) + H2O = H30* (ac) + A (ac) a. ¿Cuál es el valor de su constante de disociación ácida, Ka?1 answer -
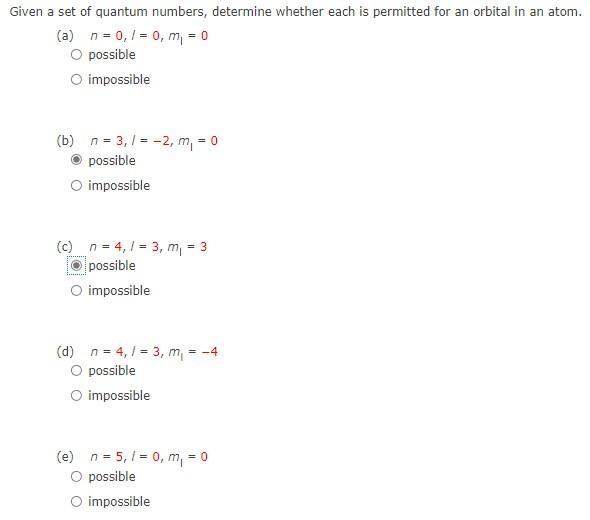
Given a set of quantum numbers, determine whether each is permitted for an orbital in an atom. (a) n = 0, 1 = 0, m = 0 possible impossible (b) n = 3,1 = -2, m, = 0 possible impossible (c) n = 4,1 = 3,1 answer -
A 0.10 solution of a weak monoprotic acid (HA) has a pH of 2.39 a) What is the value of its acid dissociation constant, Ka? b) Calculate el pKa of the acid.
8. Una solución 0.10 M de un ácido débil monoprótico (HA) tiene un pH de 2.39. HA) + H2O + H2O + A (20) a. (4 ptos.) ¿Cuál es el valor de su constante de disociación ácida, ka? b. (1 pto.) Cal1 answer -
1 answer
-
4. Calcule el cociente de reacción y determine la dirección en la que cada una de las siguientes reacciones proceder a alcanzar el equilibrio. (a) Un matraz de 1.00 L que contiene 0.0500 mol de NO (1 answer -
You want to separate compound A from compound B by flash chromatography. The following are the thin layer chromatography results of running these two compounds in different hexane/ethyl acetate system
4. Se quiere separar el compuesto A del compuesto B por "flash chromatography". Los siguientes son los resultados de cromatografía de capa fina al correr estos dos compuestos en diferentes sistemas d1 answer -
If two compounds have an Rf value of 0.50 and 0.61, how far apart are the bands from each other on the plate if the solvent front reached a distance of 15 cm?
Si dos compuestos tienen un valor de Rf de 0.50 y 0.61, ¿Qué tan separadas están las bandas una de otra en la placa si el frente del solvente alcanzó una distancia de 15 cm?1 answer -
What is the reason that explains the following increase in reactivity of alcohols when reacting with hydrogen halides (HCl, HBr)?
2. ¿Cuál es la razón que explica el siguiente incremento de reactividad de los alcoholes al reaccionar con haluros de hidrógeno (HCI, HBO)? CH3OH1 answer