¡Tu solución está lista!
Nuestra ayuda de expertos desglosó tu problema en una solución confiable y fácil de entender.
Mira la respuestaMira la respuesta done loadingPregunta: 6) Para un procedimiento para determinar la concentración de proteínas * en una muestra biológica, el kit indica que hay que hacer un amortiguador o buffer de fosfato con un pH6.8,525 mL,Ka=6.20X 10−8 y una concentración total de fosfatos de 0.5M. Tomando en cuenta que el peso molecular de NaH2PO4 es 137.99 g/mol (monohidrato) y el de Na2HPO4 es de 268.07
- Hay 4 pasos para resolver este problema.SoluciónPaso 1Mira la respuesta completaExplanation:
La ecuación de Henderson-Hasselbalch es una relación matemática que relaciona el pH de una solución ...
Paso 2 DesbloqueaPaso 3DesbloqueaPaso 4DesbloqueaRespuestaDesbloquea
DesbloqueaPaso 3DesbloqueaPaso 4DesbloqueaRespuestaDesbloquea
Texto de la transcripción de la imagen:
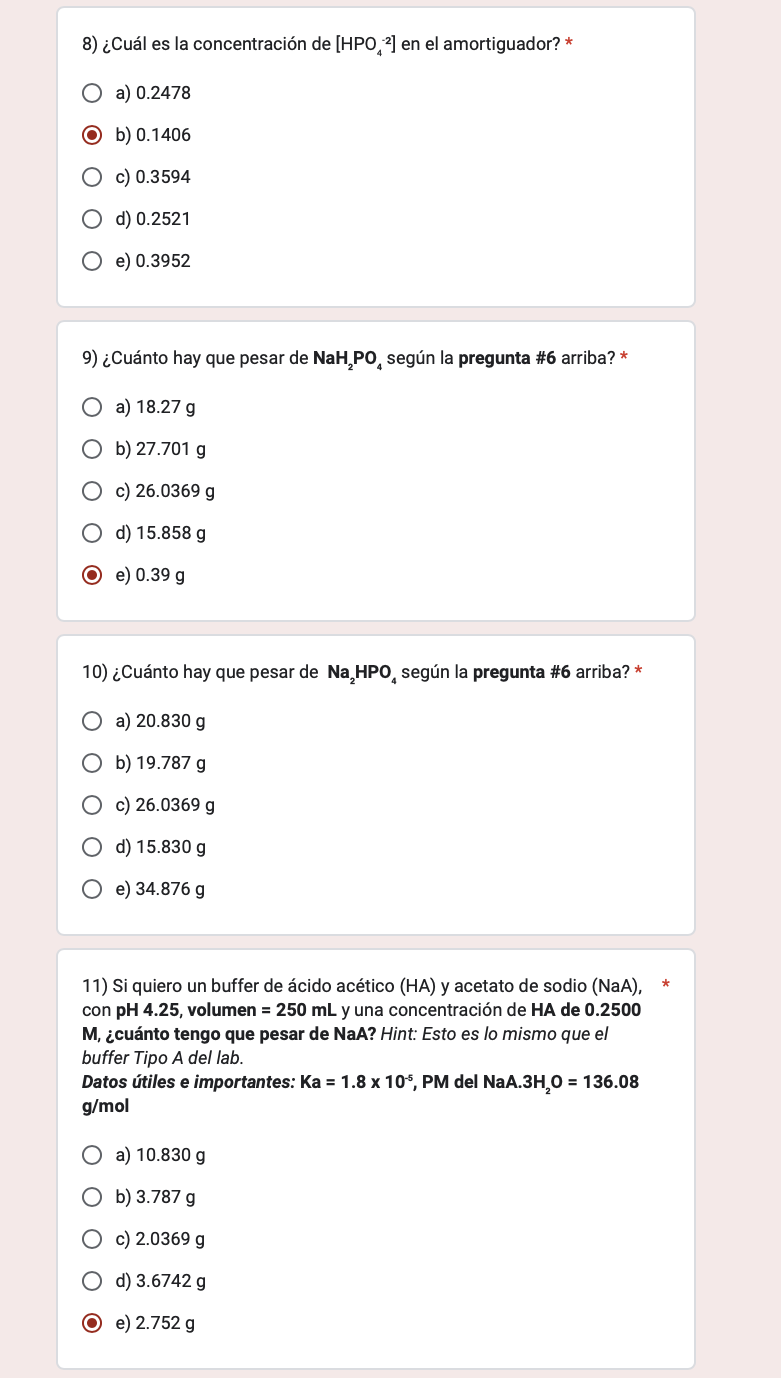
6) Para un procedimiento para determinar la concentración de proteínas * en una muestra biológica, el kit indica que hay que hacer un amortiguador o buffer de fosfato con un pH6.8,525 mL,Ka=6.20X 10−8 y una concentración total de fosfatos de 0.5M. Tomando en cuenta que el peso molecular de NaH2PO4 es 137.99 g/mol (monohidrato) y el de Na2HPO4 es de 268.07 g/mol (heptahidrato), calcule lo siguiente: ¿Cuál es la concentración de H3O+del amortiguador? Hint: Esto es similar a los cálculos del buffer TIPO B del lab. a) 6.31×10−8M b) 3.48×10−7M c) 0.25M d) 1.58×10−7M e) 18.2M 7) ¿Cuál es la razón (SEGÚN LA IMAGEN) en este amortiguador? * [HPO4−2]/[H2PO4−] a) 6.8 b) 3.48 c) 0.5 d) 0.98 e) 0.39 8) ¿Cuál es la concentración de [HPO4−2] en el amortiguador? * a) 0.2478 b) 0.1406 c) 0.3594 d) 0.2521 e) 0.3952 9) ¿Cuánto hay que pesar de NaH2PO4 según la pregunta \#6 arriba? * a) 18.27 g b) 27.701 g c) 26.0369 g d) 15.858 g e) 0.39 g
8) ¿Cuál es la concentración de [HPO4−2] en el amortiguador? * a) 0.2478 b) 0.1406 c) 0.3594 d) 0.2521 e) 0.3952 9) ¿Cuánto hay que pesar de NaH2PO4 según la pregunta \#6 arriba? * a) 18.27 g b) 27.701 g c) 26.0369 g d) 15.858 g e) 0.39 g 10) ¿Cuánto hay que pesar de Na2HPO4 según la pregunta \#6 arriba? * a) 20.830 g b) 19.787 g c) 26.0369 g d) 15.830 g e) 34.876 g 11) Si quiero un buffer de ácido acético (HA) y acetato de sodio (NaA), * con pH4.25, volumen =250mL y una concentración de HA de 0.2500 M, ¿cuánto tengo que pesar de NaA? Hint: Esto es lo mismo que el buffer Tipo A del lab. Datos útiles e importantes: Ka=1.8×10−5,PM del NaA3H2O=136.08 g/mol a) 10.830 g b) 3.787 g c) 2.0369 g d) 3.6742 g e) 2.752 g

Estudia mejor, ¡ahora en español!
Entiende todos los problemas con explicaciones al instante y pasos fáciles de aprender de la mano de expertos reales.