¡Tu solución está lista!
Nuestra ayuda de expertos desglosó tu problema en una solución confiable y fácil de entender.
Mira la respuestaMira la respuesta done loadingPregunta: 5. Una muestra de 10.00 mL de un ácido debal fue titulada con una solución de NaOH0.100M A continuación aparecen algunos de los valores del pH de la solución y el correspondiente volumen del NaOH anhadido: a) A partir de esta información se pudiera decir que el ácido es (monoprótico, diprótico o triprótico): b) Dibuje la forma que tendria la curva de
- Hay 2 pasos para resolver este problema.SoluciónPaso 1Mira la respuesta completaAl gráficar los datos se obtiene diagrama pH vs volumen de la siguiente forma donde el cambio más br...Paso 2
 DesbloqueaRespuestaDesbloquea
DesbloqueaRespuestaDesbloquea
Texto de la transcripción de la imagen:
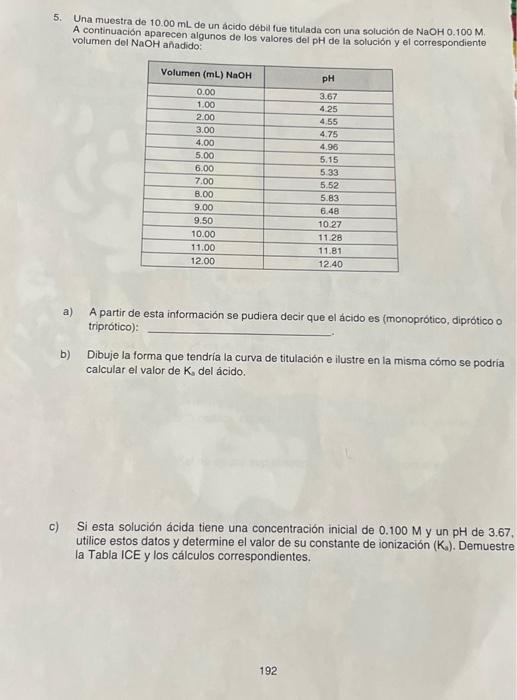
5. Una muestra de 10.00 mL de un ácido debal fue titulada con una solución de NaOH0.100M A continuación aparecen algunos de los valores del pH de la solución y el correspondiente volumen del NaOH anhadido: a) A partir de esta información se pudiera decir que el ácido es (monoprótico, diprótico o triprótico): b) Dibuje la forma que tendria la curva de titulación e ilustre en la misma cómo se podria calcular el valor de K, del ácido. c) Si esta solución ácida tiene una concentración inicial de 0.100M y un pH de 3.67 , utilice estos datos y determine el valor de su constante de ionización (Ka). Demuestre la Tabla ICE y los cálculos correspondientes.

Estudia mejor, ¡ahora en español!
Entiende todos los problemas con explicaciones al instante y pasos fáciles de aprender de la mano de expertos reales.