¡Tu solución está lista!
Nuestra ayuda de expertos desglosó tu problema en una solución confiable y fácil de entender.
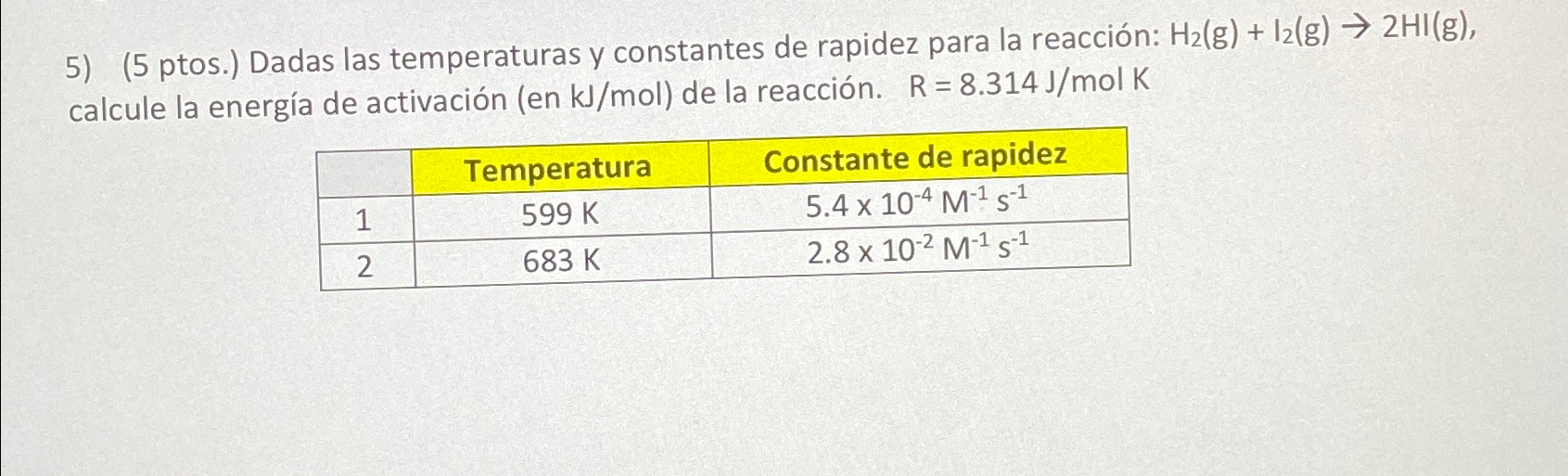
Mira la respuestaMira la respuesta done loadingPregunta: (5 ptos.) Dadas las temperaturas y constantes de rapidez para la reacción: H2(g)+I2(g)→2HI(g), calcule la energía de activación (en kJmol ) de la reacción. R=8.314JmolK
ptos. Dadas las temperaturas y constantes de rapidez para la reaccin: calcule la energa de activacin en de la reaccinolK- Hay 2 pasos para resolver este problema.SoluciónPaso 1Mira la respuesta completaExplanation:
La ecuación que relaciona dos constantes de velocidad a diferentes temperaturas viene dada según:
Don...
Paso 2 DesbloqueaRespuestaDesbloquea
DesbloqueaRespuestaDesbloquea

Estudia mejor, ¡ahora en español!
Entiende todos los problemas con explicaciones al instante y pasos fáciles de aprender de la mano de expertos reales.