¡Tu solución está lista!
Nuestra ayuda de expertos desglosó tu problema en una solución confiable y fácil de entender.
Mira la respuestaMira la respuesta done loadingPregunta: A. If for the reaction:Kci = 0.19 to 532° C. Determine the constant ofBalance for the following reactions at the same temperature:B. The
A. If for the reaction:Kci = 0.19 to 532° C. Determine the constant ofBalance for the following reactions at the same temperature:B. The equilibrium concentrations for the reaction between CO and Cl to formCalculate the constants K. and Kp given the reaction:If the initial concentration of [CH4] = 0.115 M and the equilibrium concentration of [CH2] = 0.035 M- Hay 3 pasos para resolver este problema.SoluciónPaso 1Mira la respuesta completa
Mencionemos algunos conceptos que se aplican al ajustar Kc en respuesta a cambios en la ecuación bal...
Paso 2 DesbloqueaPaso 3DesbloqueaRespuestaDesbloquea
DesbloqueaPaso 3DesbloqueaRespuestaDesbloquea
Texto de la transcripción de la imagen:
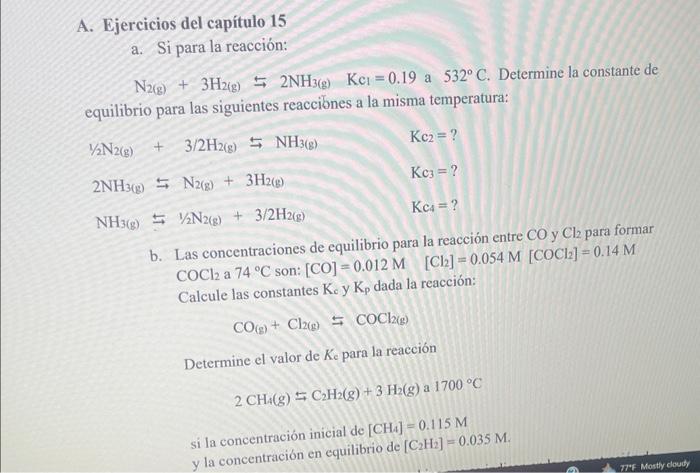
A. Ejercicios del capítulo 15 a. Si para la reacción: N2( g)+3H2( g)⇆2NH3( g)Kcl=0.19 a 532∘C. Determine la constante de equilibrio para las siguientes reacciones a la misma temperatura: 1/2 N2( g)+3/2H2( g)⇆NH3( g)2NH3( g)⇆N2( g)+3H2( g)NH3( g)⇆1/2 N2( g)+3/2H2( g)Kc2=?Kc3=?Kc=? b. Las concentraciones de equilibrio para la reacción entre COyCl2 para formar COCl2 a 74∘C son: [CO]=0.012M[Cl2]=0.054M[COCl2]=0.14M Calcule las constantes Kc y Kp dada la reacción: Determine el valor de K c para la reacción 2CH4(g)⇋C2H2(g)+3H2(g)a1700∘C si la concentración inicial de [CH4]=0.115M

Estudia mejor, ¡ahora en español!
Entiende todos los problemas con explicaciones al instante y pasos fáciles de aprender de la mano de expertos reales.