¡Tu solución está lista!
Nuestra ayuda de expertos desglosó tu problema en una solución confiable y fácil de entender.
Mira la respuestaMira la respuesta done loadingPregunta: <19 Tarea repaso temas 4.1 a 4.7 Densidad del gas y masa molar 120 La presión y la temperatura afectan la cantidad de espacio entre las moléculas de gas, lo que afecta el volumen y, por lo tanto, la densidad del gas, puesto que: densidad = volumen masa Sin embargo, la masa molar de una sustancia es una constante y se puede utilizar para identificar una
Favor de hacer tanto la A como la B
- Hay 4 pasos para resolver este problema.SoluciónPaso 1Mira la respuesta completa
Ejercicio de uso de la ley del gas ideal
Explanation:En este ejercicio hay que tener en cuenta la ley del gas id...
Paso 2 DesbloqueaPaso 3DesbloqueaPaso 4DesbloqueaRespuestaDesbloquea
DesbloqueaPaso 3DesbloqueaPaso 4DesbloqueaRespuestaDesbloquea
Texto de la transcripción de la imagen:
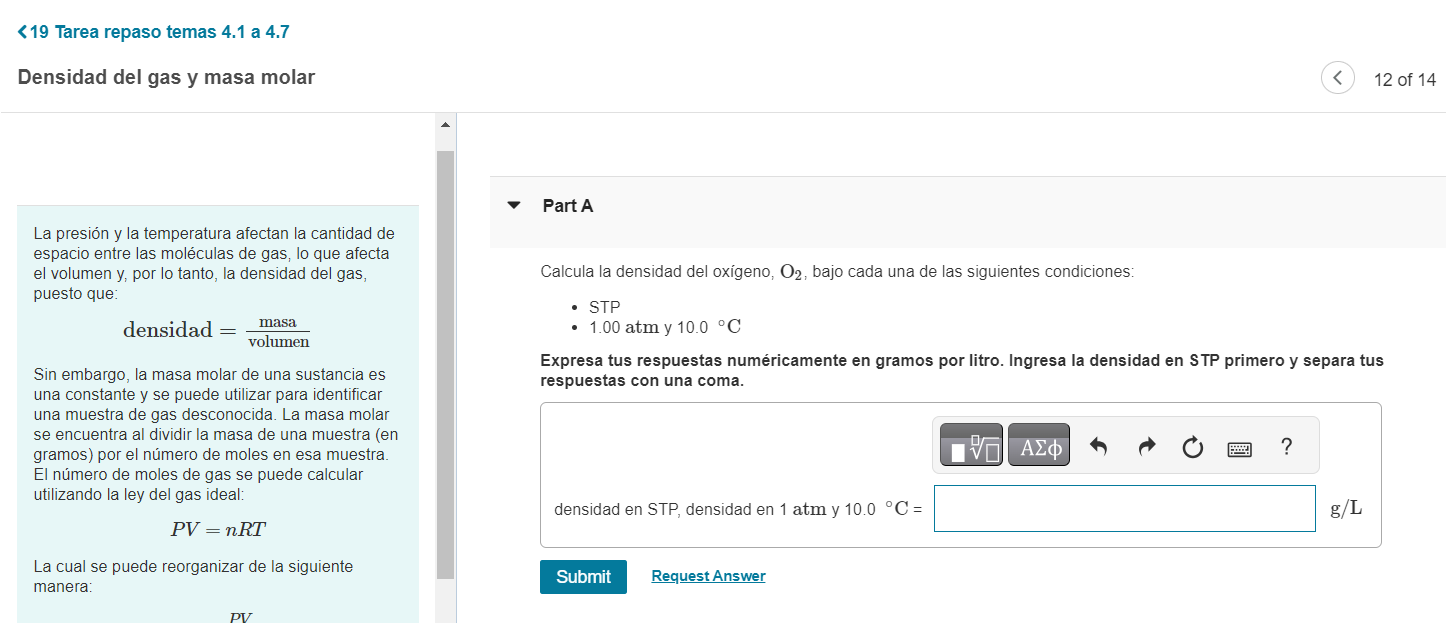
<19 Tarea repaso temas 4.1 a 4.7 Densidad del gas y masa molar 120 La presión y la temperatura afectan la cantidad de espacio entre las moléculas de gas, lo que afecta el volumen y, por lo tanto, la densidad del gas, puesto que: densidad = volumen masa Sin embargo, la masa molar de una sustancia es una constante y se puede utilizar para identificar una muestra de gas desconocida. La masa molar se encuentra al dividir la masa de una muestra (en gramos) por el número de moles en esa muestra. El número de moles de gas se puede calcular utilizando la ley del gas ideal: PV=nRT La cual se puede reorganizar de la siguiente manera: Part A Calcula la densidad del oxígeno, O2, bajo cada una de las siguientes condiciones: - STP - 1.00 atm y 10.0∘C Expresa tus respuestas numéricamente en gramos por litro. Ingresa la densidad en STP primero y separa tus respuestas con una coma.
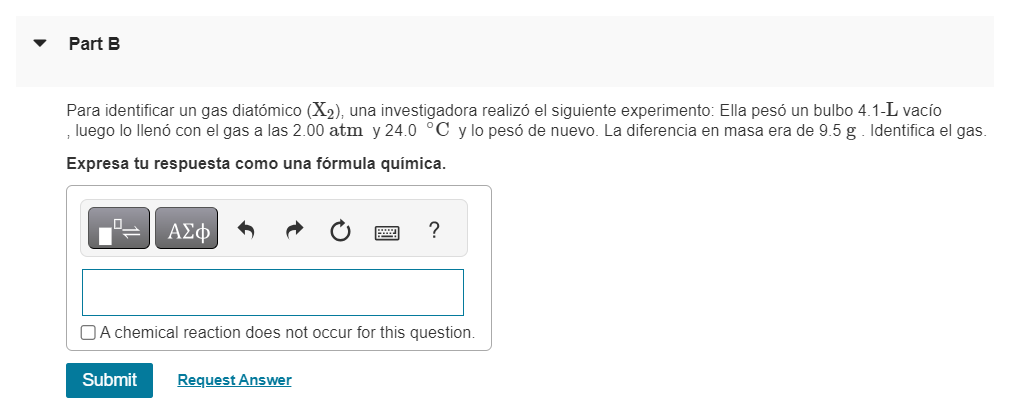
Para identificar un gas diatómico (X2), una investigadora realizó el siguiente experimento: Ella pesó un bulbo 4.1-L vacío , luego lo llenó con el gas a las 2.00 atm y 24.0∘C y lo pesó de nuevo. La diferencia en masa era de 9.5 g. Identifica el gas. Expresa tu respuesta como una fórmula química.

Estudia mejor, ¡ahora en español!
Entiende todos los problemas con explicaciones al instante y pasos fáciles de aprender de la mano de expertos reales.